コンテンツ
その他のセクション化学では、 価電子 元素の最も外側の電子殻にある電子です。特定の原子の価電子の数を見つける方法を知ることは、化学者にとって重要なスキルです。この情報によって、形成できる化学結合の種類が決まり、したがって元素の反応性が決まるからです。幸いなことに、元素の価電子を見つけるために必要なのは、元素の標準的な周期表だけです。
ステップ
パート1/2:周期表で価電子を見つける
非遷移金属
見つける 元素の周期表. これは、人類に知られているすべての化学元素をリストした多くの異なる正方形で構成された色分けされた表です。周期表は、元素に関する多くの情報を明らかにします。この情報の一部を使用して、調査している原子の価電子の数を決定します。これらは通常、化学の教科書の表紙の中にあります。ここには、オンラインで利用できる優れたインタラクティブテーブルもあります。

1から18までの元素の周期表の各列にラベルを付けます。 一般に、周期表では、単一の垂直列のすべての元素が同じ数の価電子を持ちます。周期表にまだ各列に番号が付けられていない場合は、左端に1、右端に18から始まる番号を各列に付けます。科学用語では、これらの列は要素と呼ばれます 「グループ」- たとえば、グループに番号が付けられていない周期表で作業している場合、水素(H)の上に1、ベリリウム(Be)の上に2というように、ヘリウム(He)の上に18を書くまで続けます。 。
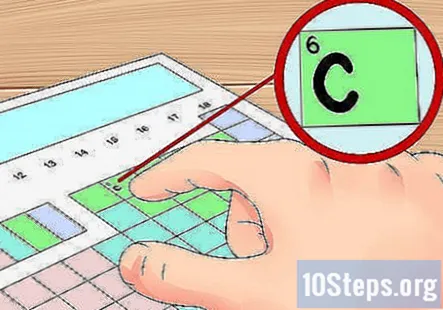
テーブルで要素を見つけます。 次に、テーブル上で価電子を見つけたい元素を見つけます。これは、化学記号(各ボックスの文字)、原子番号(各ボックスの左上の数字)、またはテーブルで利用できるその他の情報を使用して行うことができます。- 例として、非常に一般的な元素の価電子を見つけましょう。 カーボン(C)。 この元素の原子番号は6です。これは、グループ14の最上位にあります。次のステップでは、その価電子を見つけます。
- このサブセクションでは、グループ3から12で作成された長方形のブロックの要素である遷移金属を無視します。これらの要素は他の要素とは少し異なるため、このサブセクションの手順では説明しません。それらに取り組む。以下のサブセクションでこれらに対処する方法を参照してください。
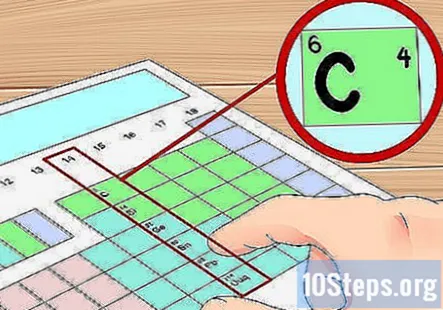
グループ番号を使用して、価電子の数を決定します。 非遷移金属のグループ番号を使用して、その元素の原子内の価電子の数を見つけることができます。ザ・ グループ番号の1の場所 これらの元素の原子内の価電子の数です。言い換えると:- グループ1:1価電子
- グループ2:2つの価電子
- グループ13:3つの価電子
- グループ14:4つの価電子
- グループ15:5価電子
- グループ16:6つの価電子
- グループ17:7つの価電子
- グループ18:8つの価電子(2つあるヘリウムを除く)
- この例では、炭素はグループ14に属しているため、炭素の1つの原子は次のようになります。 4つの価電子。
遷移金属
グループ3から12の要素を見つけます。 上記のように、グループ3から12の元素は「遷移金属」と呼ばれ、価電子に関しては他の元素とは異なる動作をします。このセクションでは、これらの原子に価電子を割り当てることがある程度不可能な場合が多いことを説明します。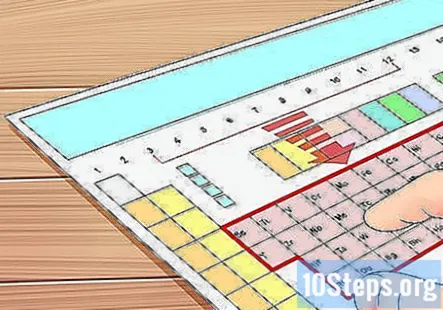
- 例として、元素73のタンタル(Ta)を選びましょう。次のいくつかのステップで、その価電子(または、少なくとも、 試してみてください に。)
- 遷移金属には、ランタニドとアクチニドのシリーズ(「希土類金属」とも呼ばれます)が含まれることに注意してください。通常、ランタンとアクチニウムで始まる、テーブルの残りの部分の下に配置される2列の元素です。これらの要素はすべてに属します グループ3 周期表の。
遷移金属には「従来の」価電子がないことを理解してください。 遷移金属が周期表の残りの部分のように実際に「機能」しない理由を理解するには、電子が原子内でどのように振る舞うかについて少し説明する必要があります。簡単な説明については以下を参照するか、この手順をスキップして正しい答えを見つけてください。
- 電子が原子に追加されると、それらはさまざまな「軌道」に分類されます。基本的には、電子が集まる核の周りのさまざまな領域です。一般に、価電子は最外殻の電子です。つまり、最後に追加された電子です。 。
- ここで説明するには少し複雑すぎる理由で、電子が最も外側に追加されたとき d 遷移金属の殻(これについては以下で詳しく説明します)では、殻に入る最初の電子は通常の価電子のように機能する傾向がありますが、その後はそうではなく、他の軌道層からの電子が代わりに価電子として機能することがあります。これは、原子がどのように操作されるかに応じて、原子が複数の価電子を持つことができることを意味します。
グループ番号に基づいて価電子の数を決定します。 繰り返しますが、調べている元素のグループ番号から、その価電子がわかります。ただし、遷移金属の場合、従うことができるパターンはありません。グループ番号は通常、価電子の可能な数の範囲に対応します。これらは: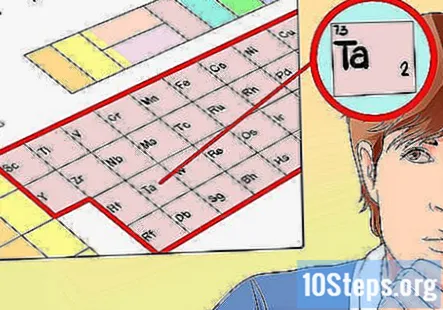
- グループ3:3つの価電子
- グループ4:2〜4価電子
- グループ5:2〜5価電子
- グループ6:2〜6価電子
- グループ7:2〜7価電子
- グループ8:2または3の価電子
- グループ9:2または3の価電子
- グループ10:2または3の価電子
- グループ11:1または2の価電子
- グループ12:2つの価電子
- この例では、タンタルはグループ5に属しているため、その間にあると言えます。 2つおよび5つの価電子、状況に応じて。
パート2/2:電子配置で価電子を見つける
電子配置の読み方を学びましょう。 元素の価電子を見つける別の方法は、電子配置と呼ばれるものを使用することです。これらは最初は複雑に見えるかもしれませんが、原子内の電子軌道を文字と数字で表すための方法にすぎず、何を見ているのかがわかれば簡単です。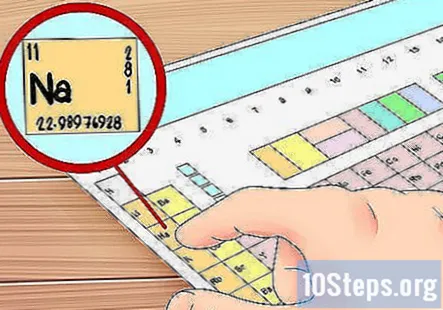
- ナトリウム(Na)元素の構成例を見てみましょう。
- 1s2s2p3s
- この電子配置は、次のような繰り返し文字列であることに注意してください。
- (数字)(文字)(数字)(文字)..。
- ...等々。ザ・ (数字)(文字) チャンクは電子軌道の名前であり、はその軌道内の電子の数です—それだけです!
- したがって、この例では、ナトリウムは 1s軌道の2つの電子 プラス 2s軌道の2つの電子 プラス 2p軌道の6つの電子 プラス 3s軌道に1つの電子。 これは合計11個の電子です—ナトリウムは元素番号11なので、これは理にかなっています。
- 各サブシェルには特定の電子容量があることに注意してください。それらの電子容量は次のとおりです。
- s:2電子容量
- p:6電子容量
- d:10電子容量
- f:14電子容量
- ナトリウム(Na)元素の構成例を見てみましょう。
調べている元素の電子配置を見つけます。 元素の電子配置がわかれば、その価電子の数を見つけるのは非常に簡単です(もちろん、遷移金属を除く)。最初から構成が与えられている場合は、次のステップにスキップできます。自分で見つける必要がある場合は、以下を参照してください。
- 周期表の最後の元素であるオガネソン(Og)の元素118の完全な電子配置を調べます。それはどの元素の中でも最も多くの電子を持っているので、その電子配置は他の元素で遭遇する可能性のあるすべての可能性を示しています。
- 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d7p
- これができたので、別の原子の電子配置を見つけるために必要なことは、最初から電子がなくなるまでこのパターンを埋めるだけです。これは思ったより簡単です。たとえば、17個の電子を持つ元素17である塩素(Cl)の軌道図を作成する場合は、次のようにします。
- 1s2s2p3s3p
- 電子の数が合計で17になることに注意してください:2 + 2 + 6 + 2 + 5 = 17。最後の軌道の数を変更するだけで済みます。最後の軌道の前の軌道が完全にいっぱいになるため、残りは同じです。 。
- 電子配置の詳細については、この記事も参照してください。
- 周期表の最後の元素であるオガネソン(Og)の元素118の完全な電子配置を調べます。それはどの元素の中でも最も多くの電子を持っているので、その電子配置は他の元素で遭遇する可能性のあるすべての可能性を示しています。
オクテット則を使用して、電子を軌道シェルに割り当てます。 電子が原子に追加されると、上記の順序に従ってさまざまな軌道に分類されます。最初の2つは1s軌道に、2つは2s軌道に、6つは2p軌道に移動します。など。遷移金属の外側の原子を扱う場合、これらの軌道は原子核の周りに「軌道殻」を形成し、連続する各殻は以前のものよりも遠くにあると言います。 2つの電子しか保持できない最初のシェルに加えて、各シェルは8つの電子を持つことができます(遷移金属を扱う場合を除く)。これは、 オクテット則。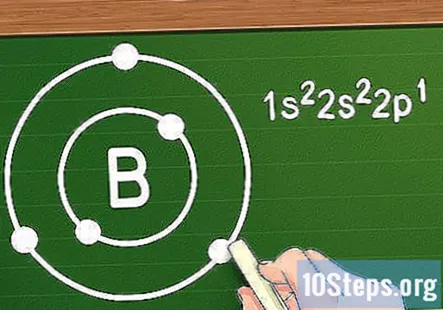
- たとえば、元素のホウ素(B)を見ているとしましょう。原子番号が5であるため、電子が5つあり、電子配置は1s2s2pのようになります。最初の軌道シェルには2つの電子しかないため、ホウ素には2つのシェルがあることがわかります。1つは2つの1s電子を持ち、もう1つは2sおよび2p軌道からの3つの電子を持ちます。
- 別の例として、塩素(1s2s2p3s3p)のような元素は、3つの軌道シェルを持ちます。1つは2つの1s電子、1つは2つの2s電子と6つの2p電子、もう1つは2つの3s電子と5つの3p電子です。
最も外側の殻の電子の数を見つけます。 元素の電子殻がわかったので、価電子を見つけるのは簡単です。最も外側の殻の電子の数を使用するだけです。外殻がいっぱいの場合(つまり、電子が8つある場合、または最初の殻の場合は2つ)、要素は不活性であり、他の要素と簡単に反応しません。ただし、繰り返しになりますが、遷移金属に関するこれらの規則に完全には準拠していません。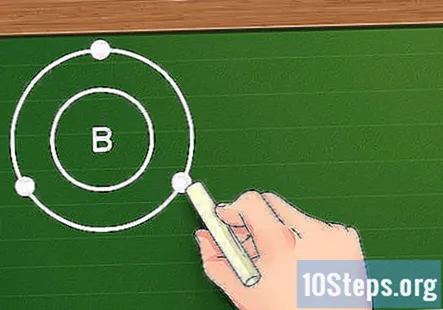
- たとえば、ホウ素を使用している場合、2番目のシェルには3つの電子があるため、ホウ素は次のようになります。 三 価電子。
テーブルの行を軌道シェルのショートカットとして使用します。 周期表の横の列は元素と呼ばれます 「生理」 表の上から順に、各期間はの数に対応します 電子殻 その期間の原子は所有しています。これをショートカットとして使用して、元素が持つ価電子の数を決定できます。電子を数えるときは、その周期の左側から開始するだけです。繰り返しになりますが、この方法では、グループ3〜12を含む遷移金属を無視する必要があります。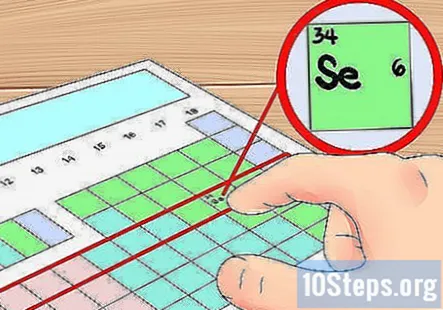
- たとえば、元素セレンは第4周期であるため、4つの軌道殻を持っていることがわかります。これは(遷移金属を無視して)第4周期の左から6番目の元素であるため、外側の4番目のシェルには6つの電子があり、セレンには6つの電子があることがわかります。 6つの価電子。
コミュニティの質問と回答
価電子をどのように計算しますか?
価電子は、元素の電子配置を決定することによって見つけることができます。その後、最外殻の電子の数は、その元素の価電子の総数を示します。
原子に33個の電子がある場合、価電子はいくつありますか?
原子がイオンでない場合、原子には33個の陽子があると言えます。これは、ヒ素である元素33であることを意味します。次に、それが遷移金属ではないことがわかったので、そのグループ番号の単位桁が5であることがわかりました。これは、5つの価電子を持っていることを意味します。
ヘリウムの原子番号を確認するにはどうすればよいですか?
陽子の数は原子番号と同じです。
電子が正電荷ではなく負電荷を得るのはなぜですか?
陽子は正電荷を持ち、強い核力によって原子核に保持されるため、原子は電子、負電荷を獲得または喪失します。これは、重力、電磁気学、弱い力、強い核力という、宇宙の4つの異なる力の1つです。陽子は互いに反発し合うが、原子核内では非常に接近しているため、強くなる必要があります(中性子とともに、強い力によっても保持されます)。強い力は非常に強いが、非常に短い距離でしか発生しないという考え方です。小さな超強力なフックを考えてください。陽子と中性子をつなぐには、星の巨大な重力、超新星、核爆発などの力が必要です。
希ガスの価電子とは何ですか?
希ガスには8つの価電子があります。これは元素にとって最も安定した状態です。
なぜ窒素は6つの価電子を持っているのにグループ15にあるのですか?
窒素はグループ5にあるため、価電子は5つしかありませんが、実際にはグループ15にありますが、これらのグループは価電子を決定する方法が異なるため、遷移金属は無視します。したがって、グループ13はグループ3などを意味します。
原子には、7つの陽子、8つのニューロン、および7つの電子があります。その原子価殻の電子の数はいくつですか?
7つの陽子を含む元素は窒素です。窒素は、原子価殻に5つの電子を持つ元素の列にあります。中性子の数は、特定の元素の価電子の数を見つけることとは無関係です。
周期表のどこに7つの外殻電子を持つ原子がありますか?
右側の不活性ガスの隣にある最後から2番目の列を見てください。
価電子とは何ですか?
価電子は、原子の最も外側の部分にある電子であり、共有したり、反応に取り入れたりすることができます。
周期表の元素の価電子数が異なるのはなぜですか?
それらは異なる化学構造を持っています。価電子は化学反応を引き起こすものです。
チップ
- 電子配置は、希ガス(グループ18の元素)を使用して、配置の開始時に軌道を代用することにより、一種の速記で記述できることに注意してください。たとえば、ナトリウムの電子配置は3s1と書くことができます。基本的にはネオンと同じですが、3s軌道にもう1つの電子があります。
- 遷移金属には、完全に満たされていない原子価サブシェルがある場合があります。遷移金属の価電子の正確な数を決定するには、この記事の範囲を超える量子論の原理が必要です。
- 周期表は国によって異なることに注意してください。したがって、混乱を避けるために、正しい更新されたものを使用していることを確認してください。
- 価電子を見つけるために、最後の軌道をいつ加算または減算するかを必ず知っておいてください。
必要なもの
- 元素の周期表
- 鉛筆
- 論文
ウィキハウでは、毎日、より安全で健康的な生活を送れるように、または健康を改善するために役立つ指示や情報にアクセスできるように努めています。現在の公衆衛生と経済危機の中で、世界が劇的に変化し、私たち全員が日常生活の変化を学び、適応しているとき、人々はこれまで以上にwikiHowを必要としています。あなたのサポートは、wikiHowがより詳細なイラスト付きの記事やビデオを作成し、信頼できるブランドの教育コンテンツを世界中の何百万もの人々と共有するのに役立ちます。今日はwikiHowに貢献することを検討してください。