著者:
Robert Doyle
作成日:
17 J 2021
更新日:
1 5月 2024

コンテンツ
化学では、「分圧」とは、ガス混合物中の各ガスが、サンプルボトル、ダイビングエアのタンク、または大気の限界などの周囲に対して及ぼす圧力を指します。混合物中の各ガスの圧力は、ガスの量、占有する体積、および温度がわかっている場合に計算できます。次に、これらの分圧を加算してガス混合物の全圧を見つけるか、最初に全圧を見つけてから分圧を見つけることができます。
ステップ
パート1/3:ガスの特性を理解する
各ガスを「理想気体」として扱います。 化学における理想気体は、分子に引き付けられることなく他の気体と相互作用する気体です。個々の分子は互いにぶつかり、ビリヤードボールのように変形することなく跳ね返ることができます。
- 理想気体の圧力は、小さな空間に圧縮されると増加し、大きな領域に膨張すると減少します。この関係は、ロバート・ボイルにちなんでボイルの法則と呼ばれています。これは数学的にk = P x V、またはより簡単に言えばk = PVとして記述されます。ここで、kは一定の関係を表し、Pは圧力を表し、Vは体積を表します。
- 圧力は、いくつかの可能な単位の1つを使用して決定できます。 1つはパスカル(Pa)で、平方メートルに加えられるニュートン力として定義されます。もう1つは、海面での地球の大気の圧力として定義される大気(atm)です。 1気圧の圧力は101,325Paに相当します。
- 理想気体の温度は、体積が増減するにつれて上昇します。この関係は、ジャックシャルルにちなんでシャルルの法則と呼ばれ、数学的にk = V / tとして記述されます。ここで、kは一定の体積と温度の関係を表し、Vは再び体積を表し、Tは温度を表します。
- この式のガス温度はケルビン度で表されます。ケルビンは、ガス温度の摂氏度数に273を加算することによって求められます。
- これらの2つの関係は、1つの方程式に組み合わせることができます。k= PV / T、これはPV = kTと書くこともできます。

ガスを測定する量を定義します。 ガスには質量と体積があります。体積は通常リットル(l)で測定されますが、質量には2つのタイプがあります。- 従来の質量はグラム、または十分に大きい質量がある場合はキログラムで測定されます。
- ガスは軽いため、分子量またはモル質量と呼ばれる別の形式の質量でも測定されます。モル質量は、ガスを構成する化合物の各原子の原子量の合計として定義され、各原子は炭素の12の値と比較されます。
- 原子と分子は小さすぎて処理できないため、ガスの量はモルで定義されます。所定のガスに存在するモル数は、質量をモル質量で割ることによって決定でき、文字nで表すことができます。
- 気体方程式の任意の定数kを、n、モル数(mol)、および新しい定数Rの積に置き換えることができます。方程式はnR = PV / TまたはPV = nRTと書くことができます。
- R値は、ガスの圧力、体積、および温度を測定するために使用される単位によって異なります。リットル単位の体積、ケルビン単位の温度、および大気圧単位の圧力を識別するために、その値は0.0821 L.atm /K.molです。これは、測定単位のスプリットバーを回避するためにL 0.0821 atm Kmolと書くこともできます。

ドルトンの分圧の法則を理解します。 化学者で物理学者のジョン・ドルトンによって開発された、原子でできている化学元素の概念を最初に発展させたドルトンの法則は、ガス混合物の全圧は混合物中の各ガスの圧力の合計であると述べています。- ドルトンの法則は、次の方程式として書くことができます。 合計 = P1 + P2 + P3...等号の後に、混合物に含まれるガスと同じ数の補遺があります。
- ドルトンの法則の方程式は、個々の分圧が不明であるが、その体積と温度がわかっているガスを扱うときに拡張できます。同じ量のガスが容器内の唯一のガスである場合、ガスの分圧は同じ圧力です。
- 分圧ごとに、理想気体の方程式を書き直して、式PV = nRTの代わりに、等号の左側にPのみを含めることができます。これを行うには、両側をVで除算します:PV / V = nRT / V。左側の2つのVは互いに打ち消し合い、P = nRT / Vのままにします。
- 次に、分圧方程式の右辺でサブスクライブされた各Pを置き換えることができます。P合計 =(nRT / V) 1 +(nRT / V) 2 +(nRT / V) 3…
パート2/3:分圧と全圧の計算

使用するガスの分圧方程式を定義します。 この計算の目的のために、3つのガスを保持する2リットルのバルーンを想定します:窒素(N2)、酸素(O2)および二酸化炭素(CO2)。各ガスは10gあり、フラスコ内の各ガスの温度は摂氏37度です。各ガスの分圧と混合物が容器に及ぼす全圧を見つける必要があります。- 分圧方程式はPになります 合計 = P 窒素 + P 酸素 + P 二酸化炭素 .
- 各ガスが及ぼす圧力を見つけようとしているので、体積と温度がわかり、質量に基づいて各ガスのモル数を見つけることができるので、この方程式を次のように書き直すことができます。合計 =(nRT / V) 窒素 +(nRT / V) 酸素 +(nRT / V) 二酸化炭素

温度をケルビンに変換します。 温度は摂氏37度なので、273を37に追加して310Kを取得します。
サンプル内の各ガスのモル数を見つけます。 ガスのモル数は、ガスの質量をそのモル質量で割ったものです。これは、化合物の各原子の原子量の合計です。
- 最初のガスの場合、窒素(N2)、各原子の原子量は14です。窒素は二原子(2つの原子の分子形態)であるため、サンプルの窒素のモル質量が28であることを確認するには、14に2を掛ける必要があります。次に、質量を除算します。グラム単位で、10 g、28で、モル数を取得します。これは、およそ0.4molの窒素になります。
- 2番目のガスの場合、酸素(O2)、各原子の原子量は16です。酸素も二原子なので、16に2を掛けると、サンプルの酸素のモル質量は32になります。10gを32で割ると、約0.3molの酸素が得られます。サンプル。
- 3番目のガスである二酸化炭素(CO2)、3つの原子を持っています:1つの炭素、12の原子量; 2つの酸素。それぞれの原子量は16です。モル質量として12+ 16 + 16 = 44の3つの重みを追加します。 10 gを44で割ると、約0.2molの二酸化炭素が得られます。

値をモル、体積、温度に置き換えます。 私たちの方程式は次のようになります:P合計 =(0.4 * R * 310/2) 窒素 +(0.3 * R * 310/2) 酸素 +(0.2 * R * 310/2) 二酸化炭素.- 簡単にするために、値に付随する測定単位は省略しています。これらの単位は、計算を行った後にキャンセルされ、圧力の報告に使用している測定単位のみが残ります。
定数Rの値を代入します。 大気圧の部分圧力と全圧がわかるので、0.0821 atm L /K.molのR値を使用します。方程式の値を代入すると、Pが得られます。合計 =(0,4 * 0,0821 * 310/2) 窒素 + (0,3 *0,0821 * 310/2) 酸素 + (0,2 * 0,0821 * 310/2) 二酸化炭素 .
各ガスの分圧を計算します。 値が設定されたので、次は計算を行います。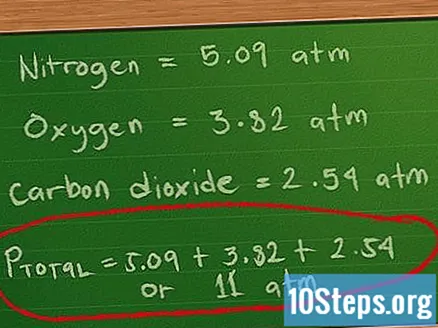
- 窒素の分圧については、0.4molに0.0821定数と310Kの温度を掛けてから、2リットルで割ります。0.4 * 0.0821 * 310/2 = 5、09atm。
- 酸素分圧の場合、0.3molに0.0821定数と310K温度を掛けてから、2リットルで割ります。0.3 * 0.0821 * 310/2 = 3、82 atm、およそ。
- 二酸化炭素の分圧については、0.2molに0.0821定数と310Kの温度を掛けてから、2リットルで割ります。0.2 * 0.0821 * 310/2 = 2.54 atm、およそ。
- ここで、これらの圧力を追加して、全圧を求めます。P合計 = 5.09 + 3.82 + 2.54、または約11.45atm。
パート3/3:全圧、次に分圧の計算
前と同じように分圧方程式を定義します。 ここでも、2リットルのフラスコに3つのガスが含まれていると仮定します。窒素(N2)、酸素(O2)、および二酸化炭素(CO2)。各ガスは10gあり、フラスコ内の各ガスの温度は摂氏37度です。
- ケルビンの温度はまだ310であり、以前と同様に、約0.4 molの窒素、0.3 molの酸素、0.2molの二酸化炭素があります。
- 同様に、大気中の圧力も検出されるため、定数Rには0.0821 atm L /K.molの値を使用します。
- したがって、この時点でも分圧方程式は同じように見えます。P合計 =(0,4 * 0,0821 * 310/2) 窒素 + (0,3 *0,0821 * 310/2) 酸素 + (0,2 * 0,0821 * 310/2) 二酸化炭素.
サンプル内の各ガスのモル数を加算して、ガス混合物の総モル数を求めます。 ガス中の各サンプルの体積と温度は同じであるため、各モル値に同じ定数を掛けることは言うまでもなく、数学の分配法則を使用して方程式をPとして書き直すことができます。合計 = (0,4 + 0,3 + 0,2) * 0,0821 * 310/2.
- 0.4 + 0.3 + 0.2 = 0.9molの混合ガスを追加します。これにより、Pの方程式がさらに単純化されます。 合計 = 0,9 * 0,0821 * 310/2.
混合ガスの全圧を計算します。 0.9 * 0.0821 * 310/2 = 11.45molを掛けると約。
全混合物中の各ガスの割合を見つけます。 これを行うには、各ガスのモル数を総モル数で割ります。
- 0.4 molの窒素があるため、サンプルの0.4 / 0.9 = 0.44(44%)になります。
- 0.3 molの窒素があるため、サンプルの0.3 / 0.9 = 0.33(33%)になります。
- 0.2 molの二酸化炭素があるため、サンプルの0.2 / 0.9 = 0.22(22%)になります。
- 上記のおおよそのパーセンテージの合計はわずか0.99ですが、実際の小数は繰り返されているため、実際の合計は小数の後の9の一連の繰り返しです。定義上、これは1、つまり100%と同じです。
各ガスの比例値に全圧を掛けて分圧を求めます。
- 0.44 * 11.45 = 5.04atmを掛けます。
- 0.33 * 11.45 = 3.78 atmを掛けると、およそ。
- 0.22 * 11.45 = 2.52 atmを掛けると、およそ。
チップ
- 最初に分圧を見つけ、次に全圧を見つけ、最初に全圧を見つけ、次に分圧を見つけることによって、値の小さな違いに気付くでしょう。値を理解しやすくするために小数点以下1桁または2桁に丸めるため、指定された値は概算値として表示されていることに注意してください。四捨五入せずに電卓を使用して計算を行う場合、2つの方法の間にわずかな不一致がある場合は気付くでしょう。
警告
- 部分的なガス圧の知識は、ダイバーにとって生死にかかわる問題になる可能性があります。酸素分圧が低すぎると意識を失って死に至る可能性があり、水素分圧または酸素分圧が非常に高いと有毒になる可能性があります。
必要な材料
- 電卓;
- 原子量/モル質量の参考書。